Полиморфизм генов фолатного цикла при беременности

27 декабря 2017 г.
Как только у женщины появляются мысли стать мамой, то она обращается в женскую консультацию для полного обследования. И в первую очередь врач назначает фолиевую кислоту. Насколько важна роль этого витамина для организма, что такое фолатный цикл и в чем заключается опасность при полиморфизме генов?
Полиморфизмы генов фолатного цикла: что это такое?
Для начала разберемся, что такое полиморфизм генов. Гены у разных людей похожи, но имеют небольшие нюансы, которые и отличают нас друг от друга. Эти нюансы, различия и называются полиморфизмами.
Причиной полиморфизма генов являются изменения отдельных участков в молекуле ДНК, что приводит к изменению свойств гена (иногда в лучшую, а иногда — в худшую сторону). Некоторые изменения ведут к генетическим заболеваниям, другие не влекут за собой болезни, но являются фактором предрасположенности к ряду патологий.
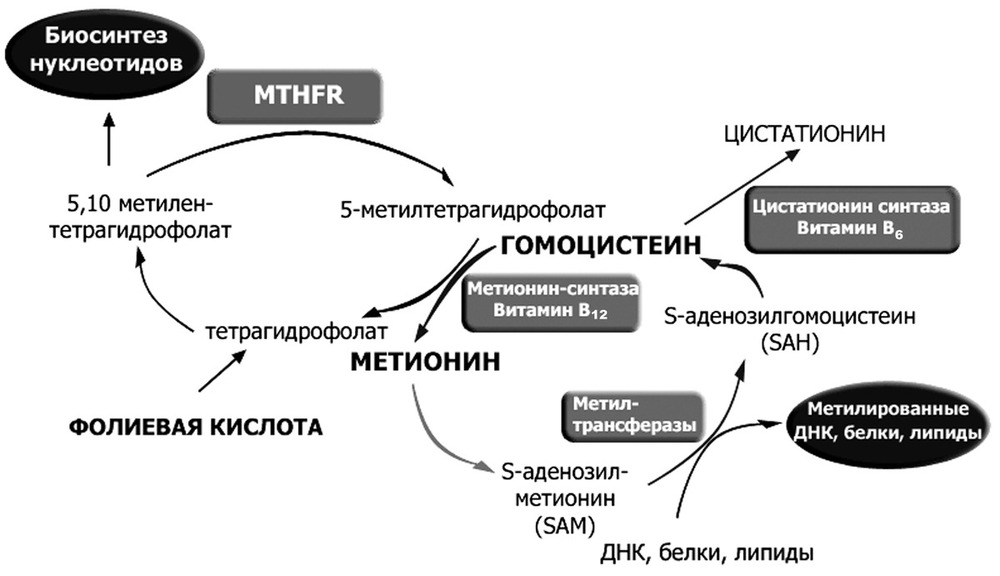
А что же такое фолатный цикл? Фолатный цикл – это совокупность процессов, в результате которых при помощи ферментов и коферментов из гомоцистеина появляется незаменимая аминокислота метионин.
Ферменты — это вещества, ускоряющие биохимические процессы в организме. В фолатном цикле принимают участие 3 фермента:
- метилентетрагидрофолатредуктаза MTHFR (для перевода фолиевой кислоты в активную форму);
- метионин-синтаза-редуктаза MTRR (влияет на активность метионин-синтазы);
- метионин-синтаза MTR (осуществляет превращение гомоцистеина);
Коферменты — это производные витаминов, необходимые для функционирования ферментов.
Коферментами являются фолаты, а для обмена фолатов необходимы витамины:
- В9 (фолиевая кислота);
- В6 (пиридоксин);
- В12 (цианокобаламин).
Фолатный цикл обеспечивает нормальное функционирование органов и систем. При мутации в генах происходит замена одного нуклеотида на другой, изменения числа повторяющихся фрагментов ДНК. Это все ведет к изменению биохимических свойств фермента и его функции, в результате чего нарушается превращение гомоцистеина в метионин.
Сбой в фолатном цикле влечет за собой увеличение концентрации в крови гомоцистеина, оказывающего на организм токсическое, атерогенное и тромбофиличское действие. Иными словами, возрастает риск некоторых осложнений беременности (например, гестоза или отслоения плаценты) и возникновения дефектов у плода.
Из-за чего может нарушиться метаболизм гомоцистеина и произойти сбой в фолатном цикле?
- генетические дефекты ферментов;
- дефицит витаминов вследствие недостаточного поступления с пищей или на фоне приема лекарственных средств (эстрогенсодержащих оральных контрацептивов, цитостатиков, противоэпилептических средств).
Кроме того, повышенный уровень гомоцистеина может быть при хронических заболеваниях: почечной недостаточности, анемии, псориазе, гипотиреозе; злокачественных опухолях яичников, молочной и поджелудочной желез.
Информация о ферментах фолатного цикла (MTHFR, MTRR, MTR) содержится в генах, которые именуются генами фолатного цикла. Эти гены могут иметь свои особенности у каждого человека — полиморфизмы. Исследование полиморфизмов в таких генах способно выявить, есть ли в конкретном случае риск нарушения фолатного цикла.
Важно! Не все полиморфизмы в генах фолатного цикла могут приводить к повышению гомоцистеина.
Диагностика полиморфизмов генов фолатного цикла
Исследование на полиморфизм генов фолатного цикла проводят методом полимеразной цепной реакции. Кровь для анализа лучше сдавать утром натощак, последний прием пищи должен быть накануне вечером.
Расшифровку данных полиморфизма генов фолатного цикла (MTR, MTRR, MTHFR) проводит только врач. Даже при выявленном полиморфизме не надо отчаиваться — это говорит только о предрасположенности к заболеванию и не означает, что в течение беременности обязательно будут осложнения.
Полиморфизмы генов фолатного цикла: в чем риск для матери и плода?
Уровень гомоцистеина при нормально протекающей беременности чуть понижается, составляя 4,6-12,4 мкмоль/л, и восстанавливается только после родов. Но при нарушениях в фолатном цикле он повышается и может оказывать токсическое, тромбофилическое и атерогенное действие.
Все это приводит к развитию различных патологических процессов со стороны матери и плода:
- угроза прерывания беременности;
- неудачное ЭКО;
- неразвивающаяся беременность;
- фетоплацентарная недостаточность;
- хроническая внутриутробная гипоксия плода;
- поздний гестоз;
- внутриутробная задержка роста и развития плода;
- пороки развития плода (дефекты нервной трубки, деформация лицевого скелета с незаращением неба и верхней губы, анэнцефалия);
- повышается риск развития синдрома Дауна.
Планирование беременности при полиморфизмах генов фолатного цикла
При планировании беременности важно выявить возможные хромосомные аномалии, в том числе носительство полиморфизма генов гемостаза и фолатного цикла.
Чтобы исключить наличие какой-либо патологии, обязательно надо посетить акушера-гинеколога. При опросе врач досконально соберет анамнез и при необходимости назначит дополнительное обследование, консультацию генетика.
Уровень гомоцистеина проверяют, если:
- предыдущие беременности завершились неблагоприятным исходом;
- у женщины повышенная свертываемость крови;
- у родственников будущей мамы были тромбозы, инфаркты или инсульты до 50 лет.
Важно! В течение 2-3 месяцев до зачатия всем женщинам совместно с партнером рекомендуют пропить фолиевую кислоту в профилактической дозе 0,4 мг/сутки.
Ведение беременности при полиморфизмах генов фолатного цикла
При наступлении беременности фолиевую кислоту продолжают пить до 12 недель включительно, что обеспечивает снижение риска нарушений со стороны нервной системы плода. Витамин выпускается в таблетках по 1 мг, назначают по 1 таб/сутки.
При полиморфизме дозировка может увеличиваться до 5 мг/сутки, а прием продолжают в течение всей беременности совместно с витаминами группы В. В критические сроки проводят дополнительную терапию.
Врач-генетик может порекомендовать принимать не обычный В9, а фолиевую кислоту в активной форме. В чем разница? Дело в том, что в чистом виде фолиевая кислота организмом не усваивается — для этого она должна преобразоваться в определенную форму — метилфолат. При мутации некоторых генов процесс превращения В9 в усвояемую форму нарушен, поэтому обычная фолиевая кислота усваивается плохо. В этом случае препаратом выбора становится ее активная форма — L-метилфолат, который легко всасывается в кровь без каких-либо преобразований.
Рекомендуют употреблять больше пищи с витамином В9 – шпинат, брокколи, горошек, авокадо, банан, арахис, бобовые, белый рис, хлеб из муки грубого помола, печень, мёд, томатный и апельсиновый соки.
В обязательном порядке контролируют уровень гомоцистеина в динамике, коагулограмму.
Врач-гинеколог о гомоцистеине при планировании беременности.
Роды при полиморфизмах генов фолатного цикла
В большинстве случаев на фоне профилактических мероприятий и проводимой терапии роды проходят хорошо.
Но могут быть следующие осложнения:
- преждевременные роды;
- преэклампсия, когда показано оперативное вмешательство в экстренном порядке;
- преждевременная отслойка нормально расположенной плаценты;
- кровотечение.
Главное, не переживайте и соблюдайте все рекомендации.
В послеродовом периоде до окончания кормления грудью продолжайте прием фолиевой кислоты по 0,4-1 мг/сутки.
Владлена Размерица, акушер-гинеколог, специально для Mirmam.pro

Фолиевая кислота в продуктах
Фолацин и фолиевая кислота: делаем правильный выбор

Путешествия во время беременности: польза или вред?

Как похудеть во время беременности, не навредив ребенку?
Источник
Исследование полиморфизма гена метилентетрагидрофолатредуктазы (MTHFR) имеет прогностическое значение и позволяет определить риск развития онкологических и сердечно-сосудистых заболеваний, а также дефектов внутриутробного развития во время беременности из-за нарушения обмена фолиевой и кислоты и гипергомоцистеинемии, оценить вероятность патологии у потомства.
Материал для исследования: плазма крови.
Метод определения: молекулярно-генетический анализ
Анализ мутаций в генах фолатного цикла — метилентетрагидрофолатредуктазы (MTHFR), редуктазы (MTRR) и метионин синтазы (MTR) позволяет определить предрасположенность к фетоплацентарной недостаточности, незаращению нервной трубки, нерасхождению хромосом в мейозе и другим патологиям плода, несовместимых с жизнью. Эти мутации связаны со снижением уровня фолатного статуса и развитием витамин-дефицитного состояния по фолиевой кислоте. Во время беременности у женщин с мутациями в этих генах отмечается снижение концентрации фолатов не только внутри эритроцитов, но и в плазме крови. Выявление таких мутаций является показанием к специальному курсу приема фолиевой кислоты.
Ген MTHFR кодирует аминокислотную последовательность фермента метилентетрагидрофолатредуктазы (МТГФР), играющего ключевую роль в метаболизме фолиевой кислоты. Дефицит МТГФР приводит к снижению метилирования ДНК, что приводит к активизации многих клеточных генов, в том числе ? онкогенов. Кроме того, происходит избыточное накопление гомоцистеина ? промежуточного продукта синтеза метионина. В случае сниженной активности МТГФР во время беременности усиливается влияние тератогенных и мутагенных факторов внешней среды.
Полиморфизм гена связан с заменой нуклеотида цитозина (С) на тимин (Т), что приводит к замене аминокислотного остатка аланина на валин в позиции 223, в участке молекулы фермента, ответственного за связывание фолиевой кислоты. У лиц, гомозиготных по данному варианту (генотип Т/Т) фермент МТГФР проявляет чувствительность к температуре (термолабильность) и теряет свою активность примерно на 65%.
Вариант Т связан с четырьмя группами многофакторных заболеваний: сердечно-сосудистыми, дефектами развития плода, колоректальной аденомой и раком молочной железы и яичников. У женщин с генотипом Т/Т во время беременности дефицит фолиевой кислоты может приводить к дефектам развития плода, в том числе, незаращению нервной трубки. У носителей этого генотипа высок риск развития побочных эффектов при приеме некоторых лекарственных препаратов, используемых в раковой химиотерапии, например, метотрексата. Неблагоприятное воздействие варианта Т полиморфизма сильно зависит от внешних факторов — низкого содержания в пище фолатов, курения, приема алкоголя. Назначение фолиевой кислоты может значительно снизить риск последствий данного варианта полиморфизма.
Варианты заключения:
C/C — нормальный вариант полиморфизма в гомозиготной форме;
C/T — гетерозиготная форма полиморфизма;
T/T — мутантный вариант полиморфизма, связанный с увеличением риска заболеваний, в гомозиготной форме
Частота встречаемости варианта Т полиморфизма в популяции: Т/Т ? 10-16%, С/Т ? 56%. Преобладающий генотип в популяции: (С/Т).
Второй вариант полиморфизма гена MTHFR связан с точечной заменой нуклеотида аденина (А) на цитозин (С), что приводит к замене аминокислотного остатка глутаминовой кислоты на аланин в позиции 429, относящейся к регулирующей области молекулы фермента. У лиц, гомозиготных и гетерозиготных по данному варианту полиморфизма отмечается некоторое снижение активности МТГФР. Это снижение обычно не сопровождается изменением уровня гомоцестеина в плазме крови, однако сочетание мутантного аллеля E429C с аллелем 677T приводит к снижению уровня фолиевой кислоты. При этом риск дефектов развития невральной трубки повышается в 2 раза. Жизнеспособность плодов, имеющих одновременно обе мутации, также снижена. Назначение фолиевой кислоты может значительно улучшить показатели риска последствий мутаций.
Варианты заключений:
А/А — нормальный вариант полиморфизма в гомозиготной форме;
А/С — гетерозиготная форма полиморфизма;
C/C — мутантный вариант полиморфизма, связанный с увеличением риска нарушений, в гомозиготной форме
Частота встречаемости варианта С полиморфизма в популяции: С/С — 3-13%, А/С — 45-55%. Преобладающий генотип в популяции: (А/А)
Ген MTRR кодирует аминокислотную последовательность фермента метионин синтазы редуктазы (МСР), играющего важную роль в синтезе белка и участвующего в большом количестве биохимических реакций, связанных с переносом метильной группы. Одной из функций МСР является обратное превращение гомоцистеина в метионин.
Полиморфизм гена MTRR связан с аминокислотной заменой в молекуле фермента МСР. В результате этой замены функциональная активность фермента снижается, что приводит к повышению риска нарушений развития плода — дефектов невральной трубки. Влияние полиморфизма усугубляется дефицитом витамина В12. При сочетании полиморфизма гена MTRR с полиморфизмом в гене MTHFR риск spina bifida увеличивается.
Варианты заключений:
A/A — нормальный вариант полиморфизма в гомозиготной форме;
A/G — гетерозиготная форма полиморфизма;
G/G — мутантный вариант полиморфизма, связанный с увеличением риска заболеваний, в гомозиготной форме
Частота встречаемости варианта G полиморфизма в популяции: G/G — 15-25%, A/G — 40-50%. Преобладающий генотип в популяции: (A/G)
Ген MTR кодирует аминокислотную последовательность фермента метионин синтазы (МС) — одного из ключевых ферментов обмена метионина, катализирующего образование метионина из гомоцистеина путем его реметиляции. В качестве кофактора в этой реакции принимает участие витамин В12 (кобаламин).
Полиморфизм гена MTR связан с аминокислотной заменой (аспарагиновой кислоты на глицин) в молекуле фермента МС. В результате этой замены функциональная активность фермента изменяется, что приводит к повышению риска синдрома Дауна у плода. Влияние полиморфизма усугубляется повышенным уровнем гомоцистеина.
Варианты заключений:
A/A — нормальный вариант полиморфизма в гомозиготной форме;
A/G — гетерозиготная форма полиморфизма;
G/G — мутантный вариант полиморфизма, связанный с увеличением риска заболеваний, в гомозиготной форме
Показания к назначению анализа:
Выявление гипергомоцистинемии у консультирующегося;
Рождение ребенка с изолированными пороками пороками нервной трубки, сердца или урогенитального тракта;
Рождение ребенка с хромосомными синдромами (при нормальном кариотипе родителей);
Наличие у консультирующегося ИБС, артериальной гипертонии;
Наличие у консультирующегося родственников I и II степени родства ИБС, артериальной гипертонии;
Невынашивание и другие осложнения, связанные с беременностью;
Плановая подготовка к беременности
Источник
Фолиевая кислота – водорастворимый витамин B9, необходимый для роста и развития кровеносной и иммунной систем. Недостаток фолиевой кислоты может вызвать мегалобластную анемию у взрослых, а при беременности повышает риск развития дефектов нервной
трубки. Производные фолиевой кислоты называются фолатами. Животные и человек не синтезируют фолиевую кислоту, получая ее в основном вместе с пищей. Фолиевая кислота в больших количествах содержится в зеленых овощах с листьями, бобовых, в хлебе из муки грубого помола, дрожжах, печени. Во многих странах законодательство обязывает производителей мучных продуктов обогащать зерна фолиевой кислотой.
Группа соединений фолатов играет ведущую роль в широком спектре жизненно важных процессов:
- стимулирует эритропоэз;
- участвует в синтезе аминокислот, нуклеиновых кислот, пуринов, пиримидинов, витаминов;
- участвует в обмене холина, гистидина;
- является важным сопутствующим фактором в метилировании ДНК и РНК;
- способствует регенерации мышечной ткани;
- влияет на развитие быстрорастущих тканей (кожа, оболочки желудочно-кишечного тракта,
- костный мозг);
- выполняет защитную функцию при беременности по отношению к действию на плод тератогенных и повреждающих факторов;
- способствует нормальному созреванию и функционированию плаценты;
- фолиевая кислота имеет эстрогеноподобное действие, что позволяет снижать прием гормонов при заместительной гормональной терапии.
Данные функции реализуются в процессе метаболизма фолатов, который составляет основу фолатного цикла.
Фолатный цикл – каскадный процесс, контролируемый ферментами, которые в качестве коферментов имеют производные фолиевой кислоты. Ключевым этапом в данном процессе является синтез метионина из гомоцистеина. Это достигается в процессе превращения фолатов: восстановления 5,10-метилентетрагидрофолата до 5-метилтетрагидрофолата, несущего метильную группу, которая необходима для превращения гомоцистеина в метионин. Восстановление фолатов происходит при участии фермента метилентетрагидрофолат-редуктазы (MTHFR). Метильная группа переносится на B12, который затем отдает ее гомоцистеину, образуя метионин с помощью фермента метионин-синтазы (MTR). Однако в некоторых случаях В12 может окисляться, что приводит к подавлению метионин-синтазы. Для поддержания активности фермента необходимо восстановительное метилирование с помощью фермента метионин-синтаза-редуктазы (MTRR).
Нарушение фолатного цикла приводит к накоплению гомоцистеина в клетках и повышению общего уровня гомоцистеина в плазме крови. Главной формой фолата в плазме является 5-метилтетрагидрофолат, несущий на себе метильную группу, которая необходима для превращения гомоцистеина в метионин. Поскольку кобаламин (витамин B12) служит акцептором метильной группы 5-метилтетрагидрофолата, дефицит этого витамина приводит к «ловушке для фолата». Это тупиковый путь метаболизма, поскольку метилтетрагидрофолат не может восстанавливаться до тетрагидрофолата и возвращаться в фолатный пул.
Это приводит к истощению запаса метионина и выбросу в кровь избытка гомоцистеина, который
обладает атерогенным действием, гипертензивными свойствами, повышает гиперагрегацию тромбоцитов.
Кроме того, гомоцистеин свободно проходит через плаценту и оказывает тератогенное и фетотоксическое действие.
Нарушение метаболизма фолатов и повышение уровня гомоцистеина обусловливают повышенный
риск развития патологических процессов:
- осложнения беременности (фетоплацентарная недостаточность, преэклампсия, преждевременная отслойка нормально расположенной плаценты (ПОНРП), замершая беременность,
- внутриутробная гибель плода);
- пороки развития плода (незаращение нервной трубки (spina bifida), анэнцефалия, деформации лицевого скелета, синдром Дауна, пороки сердца);
- сердечно-сосудистые заболевания (ишемическая болезнь сердца, инфаркт миокарда, атеросклероз, атеротромбоз);
- канцерогенез (колоректальная аденома, рак молочной железы и яичника, острый лимфолейкоз у взрослых);
- усиление побочных эффектов при химиотерапии.
Нарушения фолатного цикла не оказывают изолированного влияния на возникновение венозных тромбозов при применении гормональной заместительной терапии и оральных контрацептивов, однако при наличии других тромбофилических полиморфизмов (особенно лейденской мутации и мутации гена протромбина: 20201 G>A) многократно усиливают их действие.
Причины нарушения фолатного цикла:
- генетические дефекты ферментов фолатного цикла MTHFR, MTR и MTRR;
- дефицит фолиевой кислоты;
- дефицит витаминов В6 и В12._
Анализ полиморфизмов в генах фолатного цикла позволяет определить предрасположенность
к указанным выше патологическим процессам и дает возможность своевременного принятия мер
посредством назначения корректирующей терапии.
Показания к назначению профиля «Генетика метаболизма фолатов»:
- повышенный уровень гомоцистеина в крови (гипергомоцистеинемия);
- невынашивание беременности, гибель плода;
- рождение ребенка с изолированными пороками нервной трубки, сердца или урогенитального тракта;
- плановая подготовка к беременности;
- наличие ИБС, артериальной гипертонии, атеросклероза или атеротромбоза;
- тромбоэмболия;
- антифосфолипидный синдром;
- семейная предрасположенность к онкологическим заболеваниям;
- назначение оральных контрацептивов и гормональной заместительной терапии;
- назначение химиотерапии.
Полиморфизм гена метионинсинтазы MTR(A2756G)
Ген MTR кодирует аминокислотную последовательность фермента метионинсинтазы — одного из ключевых ферментов обмена метионина, катализирующего образование метионина из гомоцистеина путем его реметиляции. В качестве кофактора в этой реакции принимает участие витамин В12 (кобаламин). Полиморфизм гена MTR связан с аминокислотной заменой (аспарагиновой кислоты на глицин). В результате этой замены функциональная активность фермента изменяется, что приводит к повышению риска синдрома Дауна у плода. Влияние полиморфизма усугубляется повышенным уровнем гомоцистеина.
Показания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности, мегалобластная анемия, мутация MTRR.
Биологический материал для анализа: цельная кровь, стабилизированная ЭДТА
Полиморфизм гена метилентетрагидрофолатредуктазы MTHFR(A1298C) (тератогенный фактор)
У лиц, гомозиготных и гетерозиготных по данному варианту полиморфизма отмечается некоторое снижение активности МТГФР. Это снижение обычно не сопровождается изменением уровня гомоцистеина в плазме крови, однако сочетание мутантного аллеля E429C с аллелем 677T приводит к снижению уровня фолиевой кислоты. При этом риск дефектов развития невральной трубки повышается в 2 раза. Жизнеспособность плодов, имеющих одновременно обе мутации, также снижена. Назначение фолиевой кислоты может значительно улучшить показатели риска последствий мутаций. Частота встречаемости варианта С полиморфизма в популяции: С/С — 3-13%, А/С — 45-55%, преобладающий генотип в популяции: А/А.
Показания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности, дефект невральной трубки у плода в анамнезе.
Биологический материал для анализа: цельная кровь, стабилизированная ЭДТА
Полиморфизм гена метилентетрагидрофолатредуктазы MTHFR(С677Т) (наследственная гипергомоцистеинемия)
Частота встречаемости гомозиготного носительства по данной мутации среди белого населения планеты составляет от 5 до 12 %. Гетерозиготная мутация С677Т наблюдается у 50% в популяции. Полиморфизм C677T связан, по крайней мере, с четырьмя группами многофакторных заболеваний: сердечно-сосудистыми заболеваниями (атеросклеротическое поражение сосудов, атеротромбоза и его осложнений), дефектами развития плода (дефект развития нервной трубки), колоректальной аденомой и раком молочной железы и яичника.
Показания к назначению: гипергомоцистеинемия, ИБС и инфаркт миокарда, атеросклероз и атеротромбоз, антифосфолипидный синдром, полипоз кишечника, колоректальная аденома и рак, мутации генов BRCA, цервикальная дисплазия, особенно в сочетании с папилломавирусной инфекцией.
Биологический материал для анализа: цельная кровь, стабилизированная ЭДТА
Полиморфизм гена редуктазы метионинсинтазы MTRR(A66G) (тератогенный фактор)
Ген MTRR кодирует фермент метионинсинтазу редуктазу, участвующий в большом количестве биохимических реакций, связанных с переносом метильной группы. Одной из функций МСР является обратное превращение гомоцистеина в метионин. В качестве кофактора в этой реакции принимает участие витамин В12 (кобаламин). Полиморфизм I22M A>G связан с аминокислотной заменой в молекуле фермента МСР. В результате этой замены функциональная активность фермента снижается, что приводит к повышению риска нарушений развития плода – дефектов невральной трубки. Влияние полиморфизма усугубляется дефицитом витамина В12. При сочетании полиморфизма I22M A>G гена MTRR с полиморфизмом 677C-> T в гене MTHFR риск увеличивается. Полиморфизм I22M A->G гена MTRR также усиливает гипергомоцистеинемию, вызываемую полиморфизмом 677C-> T в гене MTHFR.
Показания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности.
Биологический материал для анализа: цельная кровь, стабилизированная ЭДТА
Источник
