Носитель гомозиготного полиморфизма в гене pai 1 при беременности
Столкнулась с разными мнениями врачей по этому поводу: колоть или не колоть клексан до беременности. Но нашла несколько научных статей именно на сайтах крупных медицинских центров, которые, по-моему, многое объясняют.
Мутация ингибитора активатора плазминогена — PAI-1.
Ингибитор-1 активатора плазминогена ингибирует фибринолиз, а также является маркером воспаления. PAI -1 играет важную роль в процессе фибринолитического контроля при беременности как фактор маточно–плацентарной циркуляции. Дисбаланс маточно–плацентарного фибринолитического контроля в результате повышенной продукции PAI–1 связан не только с повышением уровня фибрина в маточных сосудах и снижением маточно–плацентарного кровотока, но также играет важную роль в снижении степени инвазии трофобласта на ранних сроках беременности. Таким образом, повышенная продукция PAI–1 создает предпосылки для развития в дальнейшем гестоза и задержки внутриутробного роста плода. Промоторный полиморфизм 4G/5G в гене PAI-1 связан с повышением уровня PAI-1 и тромбоэмболизмом. У лиц – носителей гомозиготной формы 4G/4G-мутации отмечается повышение количества и функциональной активности тромбоцитов, и как следствие, снижение фибринолитической активности. В настоящее время гомозиготная форма 4G/4G гена PAI-1 обнаруживается у 82% — 85% женщин с привычным невынашиванием беременности. Повышение уровня PAI–1 возможно вследствие полиморфизма 4G/4G в гене PAI–1, при СПКЯ или метаболическом синдроме.
Полиморфизм гена ингибитора активаторов плазминогена-1 (PAI-1) и риск развития акушерской патологии
Игорь Иванович Гузов
Ингибитор активаторов плазминогена-1 (Plasminogen Activator Inhibitor-1, PAI-1) является основным антагонистом тканевого активатора плазминогена (Tissue Plasminogen Activator, tPA) и урокиназы (uPA), которые являются активаторами плазминогена, способствующими фибринолизу (растворению тромба). Он относится к группе ингибиторов сериновых протеаз (серпинам) и называется также Серпин-1.Еще одним ингибитором активаторов плазминогена является PAI-2 (plasminogen activator inhibitor-2), секретируемый плацентой и в значительных количествах обнаруживаемый только в крови беременных женщин. Кроме того, к ингибиторам активатора плазминогена относится протеаза нексин. Однако именно PAI-1 является главным ингибитором активаторов плазминогена в организме.Если концентрация PAI-1 в крови повышается, уменьшается активность противосвертывающей системы, что приводит к повышению риска тромбозов.
Оказалось также, что вариант 4G/4G предрасполагает не только к повышению риска тромбозов, но и к ожирению и повышению уровня холестерина. Торможение фибринолиза у таких людей приводит к значительному риску летальности в результате септических инфекций, в частности, менингококковой инфекции у детей. Поскольку многие осложнения беременности, в частности, поздний токсикоз (гестоз) сопровождаются тромбозом спиральных артерий, снабжающих плаценту, выяснилось что риск гестоза у женщин, являющихся носительницами варианта 5G/4G примерно в 2 раза выше, чем у женщин-носительниц варианта 5G/5G, а у женщин-носительниц варианта 4G/4G риск гестоза был в 2 раза выше, чем при варианте 5G/4G(Yamada и сотр., 2000). Вот почему исследование полиморфизма 5G/4G стало обязательной составной частью обследования при наличии в анамнезе осложнений течения беременности (остановки развития на малых сроках, тяжелые гестозы, внутриутробная смерть плода, гипотрофия и задержка внутриутробного развития, хроническая внутриутробная гипоксия плода, преждевременное созревание плаценты). Исследование полиморфизма гена PAI-1 важно проводить и при подготовке к ЭКО, поскольку мощная гормональная терапия и огромные цифры эстрогенов, сопровождающие схемы ЭКО являются фактором, повышающих риск тромбозов в месте имплантации и ранней плацентации. Положение еще более усугубляется чрезмерным увлечением врачей ЭКО назначением глюкокортикоидных гормонов, резко повышающих тромбогенность сосудистой стенки. В случае тяжелого течении инфекций периода новорожденности при подготовке к следующей беременности может потребоваться определение генотипа мужа для прогнозирования риска повторения ситуации и принятия соответствующих профилактических мер. Оказалось также, что у мужчин, в семьях которых были случаи рака предстательной железы, генотип 4G/4G (но не генотип 5G/5G) сопровождался значительным повышением риска рака простаты (Jorgenson и сотр, 2007).
FibrinolysisСхема фибринолиза. Синие стрелки — стимуляция; красные стрелки — подавлениеРазличие в фенотипических проявлениях генотипа PAI-1 обусловлены тем, что с промотором гена 5G может связываться как активатор, так и репрессор, а с промотором гена 4G — только активатор. Поэтому ген 5G, легко включается и легко выключается, а ген 4G легко включается, но плохо выключается. Вариант 5G сопровождается повышенной активностью активаторов плазминогена, а следовательно более высокой скоростью превращения плазминогена в плазмин, что способствует более высокой активации тканевых металлопротеиназ, растворяющих соединительную ткань. Поэтому носители варианта 5G имеют повышенный риск развития аневризмы аорты по сравнению с носителями генотипа 4G. Таким образом, за каждое преимущество нужно платить, и, как говорил мой знакомый профессор из Голландии, в каждом преимуществе есть свой недостаток, а в каждом недостатке — свое преимущество. Назначение специальной профилактики во время беременности (низкодозированная ацетилсалицилловая кислота и малые дозы препаратов гепарина) позволяет практически полностью устранить риск осложнений беременности у женщин с генотипами 4G/4G и 5G/4G.
Источник
2 февраля 2019, 20:55
Мутация ингибитора активатора плазминогена — PAI-1. Ингибитор-1 активатора плазминогена ингибирует фибринолиз, а также является маркером воспаления. PAI -1 играет важную роль в процессе фибринолитического контроля при беременности как фактор маточно–плацентарной циркуляции. Дисбаланс маточно–плацентарного фибринолитического контроля в результате повышенной продукции PAI–1 связан не только с повышением уровня фибрина в маточных сосудах и снижением маточно–плацентарного кровотока, но также играет важную роль в снижении степени инвазии трофобласта на ранних сроках беременности. Таким образом, повышенная продукция PAI–1 создает предпосылки для развития в дальнейшем гестоза и задержки внутриутробного роста плода. Промоторный полиморфизм 4G/5G в гене PAI-1 связан с повышением уровня PAI-1 и тромбоэмболизмом. У лиц – носителей гомозиготной формы 4G/4G-мутации отмечается повышение количества и функциональной активности тромбоцитов, и как следствие, снижение фибринолитической активности. В настоящее время гомозиготная форма 4G/4G гена PAI-1 обнаруживается у 82% — 85% женщин с привычным невынашиванием беременности. Повышение уровня PAI–1 возможно вследствие полиморфизма 4G/4G в гене PAI–1, при СПКЯ или метаболическом синдроме. Полиморфизм гена ингибитора активаторов плазминогена-1 (PAI-1) и риск развития акушерской патологии Игорь Иванович Гузов Ингибитор активаторов плазминогена-1 (Plasminogen Activator Inhibitor-1, PAI-1) является основным антагонистом тканевого активатора плазминогена (Tissue Plasminogen Activator, tPA) и урокиназы (uPA), которые являются активаторами плазминогена, способствующими фибринолизу (растворению тромба). Он относится к группе ингибиторов сериновых протеаз (серпинам) и называется также Серпин-1.Еще одним ингибитором активаторов плазминогена является PAI-2 (plasminogen activator inhibitor-2), секретируемый плацентой и в значительных количествах обнаруживаемый только в крови беременных женщин. Кроме того, к ингибиторам активатора плазминогена относится протеаза нексин. Однако именно PAI-1 является главным ингибитором активаторов плазминогена в организме.Если концентрация PAI-1 в крови повышается, уменьшается активность противосвертывающей системы, что приводит к повышению риска тромбозов. Оказалось также, что вариант 4G/4G предрасполагает не только к повышению риска тромбозов, но и к ожирению и повышению уровня холестерина. Торможение фибринолиза у таких людей приводит к значительному риску летальности в результате септических инфекций, в частности, менингококковой инфекции у детей. Поскольку многие осложнения беременности, в частности, поздний токсикоз (гестоз) сопровождаются тромбозом спиральных артерий, снабжающих плаценту, выяснилось что риск гестоза у женщин, являющихся носительницами варианта 5G/4G примерно в 2 раза выше, чем у женщин-носительниц варианта 5G/5G, а у женщин-носительниц варианта 4G/4G риск гестоза был в 2 раза выше, чем при варианте 5G/4G(Yamada и сотр., 2000). Вот почему исследование полиморфизма 5G/4G стало обязательной составной частью обследования при наличии в анамнезе осложнений течения беременности (остановки развития на малых сроках, тяжелые гестозы, внутриутробная смерть плода, гипотрофия и задержка внутриутробного развития, хроническая внутриутробная гипоксия плода, преждевременное созревание плаценты). Исследование полиморфизма гена PAI-1 важно проводить и при подготовке к ЭКО, поскольку мощная гормональная терапия и огромные цифры эстрогенов, сопровождающие схемы ЭКО являются фактором, повышающих риск тромбозов в месте имплантации и ранней плацентации. Положение еще более усугубляется чрезмерным увлечением врачей ЭКО назначением глюкокортикоидных гормонов, резко повышающих тромбогенность сосудистой стенки. В случае тяжелого течении инфекций периода новорожденности при подготовке к следующей беременности может потребоваться определение генотипа мужа для прогнозирования риска повторения ситуации и принятия соответствующих профилактических мер. Оказалось также, что у мужчин, в семьях которых были случаи рака предстательной железы, генотип 4G/4G (но не генотип 5G/5G) сопровождался значительным повышением риска рака простаты (Jorgenson и сотр, 2007). FibrinolysisСхема фибринолиза. Синие стрелки — стимуляция; красные стрелки — подавлениеРазличие в фенотипических проявлениях генотипа PAI-1 обусловлены тем, что с промотором гена 5G может связываться как активатор, так и репрессор, а с промотором гена 4G — только активатор. Поэтому ген 5G, легко включается и легко выключается, а ген 4G легко включается, но плохо выключается. Вариант 5G сопровождается повышенной активностью активаторов плазминогена, а следовательно более высокой скоростью превращения плазминогена в плазмин, что способствует более высокой активации тканевых металлопротеиназ, растворяющих соединительную ткань. Поэтому носители варианта 5G имеют повышенный риск развития аневризмы аорты по сравнению с носителями генотипа 4G. Таким образом, за каждое преимущество нужно платить, и, как говорил мой знакомый профессор из Голландии, в каждом преимуществе есть свой недостаток, а в каждом недостатке — свое преимущество. Назначение специальной профилактики во время беременности (низкодозированная ацетилсалицилловая кислота и малые дозы препаратов гепарина) позволяет практически полностью устранить риск осложнений беременности у женщин с генотипами 4G/4G и 5G/4G.
Источник
SERPINE1 (PAI-1)
Ингибитор активатора плазминогена 1 является одним из основных компонентов антисвертывающей системы крови. Ингибитор активатора плазминогена образуется в эндотелиальных клетках, гепатоцитах, депонируется в тромбоцитах в неактивной форме. Время полужизни активной молекулы в кровотоке – около 2 часов . Основная функция ингибитора активатора плазминогена 1 – ограничить фибринолитическую активность местом расположения гемостатической пробки за счет ингибирования тканевого активатора плазминогена. Это выполняется за счет большего содержания его в сосудистой стенке по сравнению с тканевым активатором плазминогена. Таким образом, на месте повреждения активированные тромбоциты выделяют избыточное количество ингибитора активатора плазминогена 1, предотвращая преждевременный лизис фибрина.
Редко встречающийся дефицит PAI-1 вызывает усиление фибринолиза и сопровождается кровотечениями.
Концентрация PAI-1 зависит как от внешних (уровень триглицеридов , курение ), так и внутренних (генетических) факторов.
PAI является белком острой фазы . Его активность возрастает после больших
операций, тяжелых травм, инфаркта миокарда. После введения в организм
кортикостероидов, эндотоксина (бактериальный LPS) активность PAI нарастает.
Статины вызывают снижение экспрессии гена PAI-1 . Уровень тканевого
активатора плазминогена в плазме пострадавших с травматическим шоком
уменьшается в 2—3 раза, а его ингибитора в 1,8—2 раза .
Выявлено повышенное содержание PAI-1 в тучных клетках, что подтверждает
участие этого белка в патогенезе бронхиальной астмы и других IgE-
опосредованных аллергических заболеваниях . Также показано участие PAI-1 в
ремоделировании дыхательных путей.
Активность PAI в течение беременности постепенно нарастает, и в третьем
триместре концентрация PAI-2 повышается до 100 мкг/мл (определяется
иммунологическим методом), особенно при действии отягощающих беременность
факторов, а после родов возвращается к норме.
У больных инфарктом миокарда отмечено повышение активности PAI и снижение
содержания и активности тканевого активатора. Часто активность PAI повышается
у больных венозными тромбозами. Повышение PAI у таких больных в
предоперационном периоде угрожает послеоперационным тромбозом.
PAI-1 участвует в ремоделировании сосудов и репарации тканей . Показано, что
высокий уровень PAI-1 тормозит образование intima media артерий .
Полиморфизм -675 5G>4G.
Полиморфный вариант 4G затрагивает промоторную область и сопровождается
повышенной экспрессией гена и повышением уровня PAI-1 в крови . В результате
снижается активность тромболитической системы.
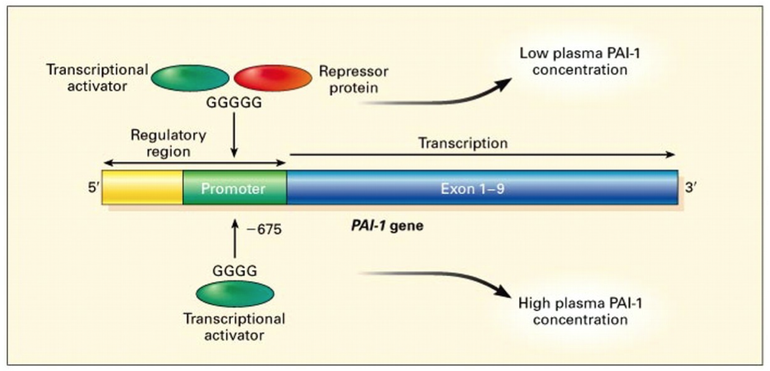
Различия в фенотипических проявлениях генотипа PAI-1 обусловлены тем, что с
промотором гена 5G может связываться как активатор, так и репрессор, а с
промотором гена 4G — только активатор. Поэтому ген 5G, легко включается и легко
выключается, а ген 4G легко включается, но плохо выключается (Рисунок 2).
Рисунок 2. Регуляция экспрессии гена PAI-1
По-видимому, на фенотипическое проявление данного полиморфизма
существенное влияние оказывает генетический фон, т.к. имеются существенные
различия в зависимости от расы и пола . У китайцев 4G аллель сильнее влияет на
уровень PAI-1 у женщин, чем у мужчин.
Популяция | Частота встречаемости генотипа, % | ||
5G/5G | 5G/4G | 4G/4G | |
Европейская | 35 | 39 | 26 |
Африканская | 58 | 33 | 9 |
Клинические проявления
• Снижение фибринолитической активности крови
• Риск тромбообразования возрастает примерно в 1,7 раза как у гомозигот, так и у гетерозигот.
Дополнительные факторы риска:
• Дефицит протеина S. Показано, что риск венозных тромбозов
увеличивается только у пациентов, имеющих дефицит протеина S и
гомозиготных по 4G аллелю.
• Избыточная масса тела
• Гипертриглицеридемия
• Сердечно-сосудистые заболевания
Для гетерозиготного состояния данного полиморфизма (4G/5G) риск
сердечно-сосудистых заболеваний возрастает незначительно .
Дополнительные факторы риска:
Ожирение
Гипертриглицеридемия
Максимальный риск сердечно-сосудистой патологии у гомозигот
наблюдается при гипертриглицеридемии .Резистентность к инсулину
Восстановление после эпизодов сердечно-сосудистых заболеваний
Носители аллеля 4G имеют повышенный риск ишемии и неблагоприятного
исхода вне зависимости от этиологии первичного эпизода (ишемический
или геморрагический) .Преэклампсия 5G/4G OR=1.49
Бронхиальная астма . Для носителей 4G аллеля характерно снижение
объема форсированного выдоха и повышение чувствительности бронхов к
гистамину у пациентов с аллергией на домашнюю пыль.
У гетерозигот 5G/4G повышен риск развития бронхиальной астмы при
аллергии на домашнюю пыль (OR=2.81) .Дополнительные факторы риска:
Генотип CD14: -159 C/C
• Данные о связи 4G аллеля с повышением риска венозной тромбоэмболии
при ГЗТ и ОК практически отсутствуют. По-видимому, большее влияние на
возникновение тромбоза в этой ситуации имеет снижение естественных
антикоагулянтов и курение .
Рекомендованные дополнительные исследования
Активность ингибитора активатора плазминогена.
Активность плазминогена.
Уровень триглицеридов
Индекс атерогенности
Уровень протеина S
Источник
Проблема синдрома привычной потери плода при- стально изучается исследователями и не теряет акту- альности в течение нескольких десятилетий. Особое внимание уделяется клеточно-молекулярным взаимо- действиям в тканях эндометрия и плаценты. Течение беременности и ее исход зависят от условий, в которых происходили имплантация и дальнейшее формирова- ние плаценты. Иммуно-эндокринные взаимодействия и ангиогенез непосредственно влияют на локальный эндометриальный гемостаз. В результате в физиологи- ческих условиях внутрисосудистый кровоток сохраня- ется за счет повышенной коагуляционной активности в периваскулярных областях и высокой фибринолити- ческой активности в просвете эндометриальных сосу- дах. В создании такого равновесия принимает участие весь комплекс плазменных факторов: активаторов и ингибиторов коагуляции и фибринолиза. В настоя- щее время известна роль генетически обусловленных дефектов гемостаза, приводящих к тромбозам, тром- боэмболиям, а также акушерским осложнениям, таким, как привычное невынашивание, неудачные попытки ЭКО, гестоз, преждевременная отслойка нормально расположенной плаценты и т.д. Целью нашего исследования явилась попытка определить роль полиморфизма гена PAI-1 в аку- шерской патологии у женщин с привычной поте- рей плода. Было обследовано 90 женщин в возрас- те от 20 до 39 лет с привычным невынашиванием. В ходе обследования сформировано 3 группы: 1 ос- новную группу составили 30 женщин с гомозигот- ным генотипом 4G/4G (PAI-1), во 2 основную груп- пу вошли 30 женщин с гетерозиготным генотипом гена PAI-1, 3 — группа сравнения была представле- на 30 пациентками, не имевшими полиморфизма в гене PAI-1. Определение аллельного полиморфизма 4G/5G в гене PAI-1 проводили методом полимераз- ной цепной реакции (ПЦР). Изучение тромбоцитар- ного звена свертывающей системы крови состояло из определения числа тромбоцитов в венозной крови, морфологической оценки внутрисосудистой актива- ции тромбоцитов по методу А.С. Шитиковой (1992). Комплексное исследование плазменно-коагуляцион- ного звена гемостаза включало такие методы, как: время свертывания венозной крови, активирован- ное время рекальцификации плазмы, протромбино- вый индекс, концентрация фибриногена, активность фактора VIII. Для оценки фибринолитической актив- ностикрови использовали метод определения лизиса эуглобулиновой фракции плазмы и фибринолитиче- скую активность цельной крови. Определение уров- ня гомоцистеина в плазме крови проводили методом иммуноферментного анализа. При анализе анамнестических данных было вы- явлено, что у 28 (31,1 %) женщин репродуктивным неудачам предшествовало прерывание первой бере- менности путем медицинского аборта, у 56,0 (62,2 %) пациенток произошли самопроизвольные выкидыши, начиная с первой беременности, у 63,0 (70,0 %) об- следованных была выявлена неразвивающаяся бере- менность. Среди инфекций половых путей чаще всего встречалась кандидозная (23,3 %), уреаплазменная (18,8 %), микоплазменная (6,6 %). Отмечались еди- ничные случаи генитального герпеса и хламидиоза. У 46,6 % женщин был выявлен хронический эндо- метрит, в 35,5 % визуализировалась эктопия шейки 8 матки, у 16,6 % пациенток обнаружены признаки хронического сальпингооофорита и миомы матки. Исследование параметров гемостаза проводилось в условиях отсутствия обострения бактериально-ви- русной инфекции в период с 15 дня менструального цикла до наступления менструации. До беременности в показателях гемостаза достоверных различий между группами не обнаружено. При беременности в I три- местре в группе женщин с гомозиготным состоянием гена PAI-1 были выявлены признаки гиперкоагуля- ции, в группе с гетерозиготным состоянием гена PAI-1 и группе сравнения отмечались нормальные параме- тры гемостаза. Во II и III триместрах гиперкоагуляция сохранялась в 16,6 % наблюдений у пациенток 1 основ- ной группы и в 10,0 % у пациенток 2 основной группы (p<0,05). Было проанализировано течение настоящей беременности у обследованных женщин. Следует от- метить, что отслойки хориона до 8 недель беременно- сти с последующим образованием ретрохориальной гематомы встречались в группе женщин с гомозигот- ным состоянием гена PAI-1 в 23,3 % случаев и сопро- вождались низкой плацентацией в I–II триместрах в 20,0 % наблюдений. В III триместре у 3 (10,0 %) па- циенток данной группы выявлено предлежание пла- центы. Признаки фето-плацентарной недостаточно- сти обнаружены в 16,6 % случаев (p<0,05) у женщин из 1 и 2 основных групп. Отеки беременных достовер- но чаще (p=0,05) встречались у женщин с наличием полиморфизма гена PAI-1, чем в группе сравнения. В настоящее время варианты полиморфизмов гена PAI-1 связывают с повышением концентрации PAI-1 в плазме. Наиболее частый полиморфизм 4G/5G ас- социируют с повышенной PAI-1 активностью, при гомозиготном носительстве 4G аллеля активность PAI-1 еще выше, что приводит к нарушению контро- ля за фибринолитической активностью, гиперкоагу- ляции и последующему тромбозу. Более углубленное изучение системы фибринолиза представляет собой научно-практический интерес и раскрывает возмож- ности для дальнейшего установления причин син- дрома привычной потери плода.
МАТЬ И ДИТЯ, Москва
XII Всероссийский научный форум, 2011
Источник

